Le passé, le présent et l’avenir : utiliser l’évolution tumorale pour améliorer la prévention, le diagnostic et le traitement du cancer
Que se passe-t-il quand un cancer qui semble avoir bien répondu au traitement réapparaît sans cesse, évoluant vers une forme plus mortelle et échappant aux diverses options thérapeutiques? Tandis que le nombre de personnes dont le cancer initial a été traité avec succès augmente progressivement, savoir comment les cancers évoluent est devenu une question centrale en recherche sur le cancer, et découvrir comment appliquer les dernières technologies pour déjouer la maladie est l’un des plus grands défis auxquels les chercheurs et les cliniciens en cancérologie sont confrontés aujourd’hui.
Cette année, l’IORC a lancé l’initiative d’oncologie adaptative pour réunir les chercheurs afin qu’ils mettent au point et utilisent de nouvelles technologies leur permettant de suivre l’évolution des tumeurs dans l’organisme et d’apprendre comment le cancer change avec le temps et échappe au système immunitaire de l’organisme et aux traitements.

Dr Lincoln Stein
Il s’agit d’une nouvelle approche que l’on peut comparer à une longue partie d’échecs aux enjeux importants. Si les cliniciens sont toujours capables de prévoir le prochain coup du cancer, celui-ci ne peut pas gagner. Cependant, prévoir ces coups exige plus qu’une « paire d’yeux » sur l’échiquier. La génomique, la pathologie, l’imagerie et d’autres disciplines doivent être mises à contribution pour que l’on puisse comprendre pleinement la voie qu’une tumeur est susceptible de prendre. L’équipe d’oncologie adaptative travaille de concert dans le but de mettre au point les technologies nécessaires pour prévoir les coups du cancer et enrayer la maladie, ce qui, en fin de compte, contribuera à empêcher que le cancer du patient devienne mortel.
« Le concept d’évolution tumorale intéresse depuis longtemps les chercheurs, mais les technologies qui permettent d’étudier de manière approfondie les tumeurs au fil du temps et de comprendre les mécanismes de leur évolution ne sont disponibles que depuis peu », explique le Dr Lincoln Stein, chef du programme d’oncologie adaptative. « Nous croyons qu’une fois que nous comprenons mieux le "plan de match" de la tumeur, c’est-à-dire la façon dont elle évolue dans le temps et l’espace, nous pouvons dès lors nous servir de cette information pour élaborer des stratégies qui tentent d’empêcher ces changements évolutifs. »
Nouvelle méthode permettant le séquençage des tumeurs au moyen d’un simple échantillon de sang
Comprendre le plan de match d’une tumeur commence au niveau du génome, où étudier la façon dont elle évolue chez le patient peut aider à mieux caractériser le cancer et prévoir le prochain coup de la tumeur. Toutefois, suivre l’évolution d’une tumeur dans l’organisme du patient nécessite de séquencer périodiquement le génome pour suivre les changements au fil du temps, afin de savoir si la tumeur est en train de devenir plus agressive ou si un cancer traité est réapparu. Pour cela, il faut effectuer plusieurs biopsies chez le patient pour obtenir des échantillons individuels à séquencer, une intervention habituellement désagréable que les patients tentent souvent d’éviter. Les chercheurs en oncologie adaptative mettent au point des méthodes qui permettent d’obtenir les échantillons nécessaires au séquençage d’une manière moins effractive que la biopsie, ce qui améliore la qualité de vie des patients et ouvre la voie à une utilisation plus généralisée des stratégies d’oncologie adaptative en pratique clinique.
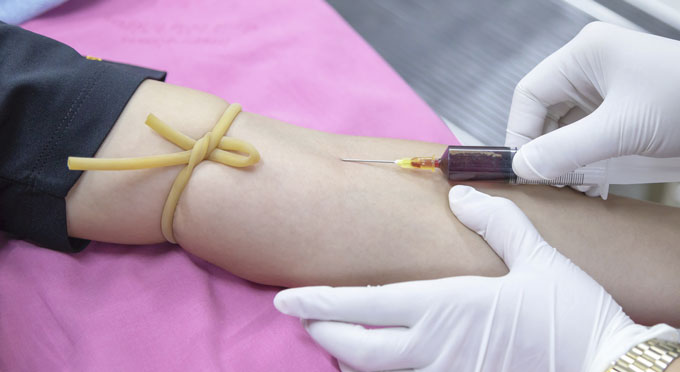
Sur le plan technique, les pas de géant qui ont été faits dans le domaine du séquençage génomique au cours de la dernière décennie rendent possible le séquençage de quantités infinitésimales d’ADN tumoral. À son tour, ce séquençage a permis, dans certains cas, de recourir à un simple échantillon de sang, appelé biopsie liquide, pour séquencer les tumeurs en utilisant l’ADN acellulaire présent dans la circulation sanguine. Cela signifie qu’il suffit aux patients de fournir des échantillons de sang à leur clinicien au lieu de subir une biopsie effractive. La possibilité de surveiller le cancer de cette manière a facilité le recours plus généralisé à la médecine de précision, une stratégie thérapeutique axée sur l’utilisation des caractéristiques spécifiques de la tumeur du patient pour le choix des traitements, et contribuera à l’élaboration de nouvelles stratégies pour surveiller et traiter le cancer avant qu’il devienne mortel.
Un autre ensemble de technologies permet aux chercheurs de séquencer le génome d’une cellule unique. À l’aide de ces outils, les chercheurs de l’IORC sont capables d’établir le profil de la combinaison précise de cellules hôtes normales, cancéreuses et réactives dans une tumeur et d’étudier de quelle façon cette combinaison évolue au fil du temps.
« Le séquençage génomique a été appliqué avec plus ou moins de succès dans le contexte de la médecine de précision. L’hétérogénéité des tumeurs signifie que même si une mutation traitable par un médicament est découverte dans le cancer d’un patient, cette mutation peut n’être présente que dans une portion des cellules tumorales, ce qui veut dire que le reste des cellules de la tumeur ne sont pas bien traitées, affirme le Dr Stein. Nous nous efforçons d’améliorer le séquençage génomique pour qu’il permette de déceler un plus grand nombre de mutations contenues dans une tumeur au moyen de technologies comme le séquençage de cellule unique. Nous aurons ainsi un portrait plus complet de la complexité de la tumeur du patient et, par conséquent, une bien meilleure idée des options thérapeutiques à privilégier. »
L’imagerie de précision révèle un autre niveau d’évolution tumorale.
Les techniques de pointe en séquençage génomique employées par les chercheurs du programme d’oncologie adaptative constituent une pièce maîtresse de l’initiative, mais ne sont qu’une des lentilles par lesquelles on observe une tumeur. « Le séquençage nous fournit l’information génétique que nous avons besoin de connaître sur une tumeur, mais on ne peut obtenir un "portrait global" de cette tumeur que si l’on est aussi en mesure de suivre son évolution au niveau structural et anatomique », dit le Dr Stein.
M. Aaron Fenster, docteur en biophysique médicale et codirecteur du programme d’imagerie en oncologie adaptative, met actuellement au point des instruments robotiques qui servent à guider avec précision les fines aiguilles à biopsie par imagerie ultrasonique. Cette méthode a l’avantage de permettre l’échantillonnage précis de différentes zones de la tumeur d’après son apparence, ce qui aide le groupe à mener ses recherches. L’équipe d’oncologie adaptative examine s’il existe un lien entre la variation de l’apparence d’une tumeur et l’hétérogénéité génomique.
Le séquençage nous fournit l’information génétique que nous avons besoin de connaître sur une tumeur, mais on ne peut obtenir un "portrait global" de cette tumeur que si l’on est aussi en mesure de suivre son évolution au niveau structural et anatomique.
- Dr. Lincoln Stein
« Selon nous, cette technologie améliorera les résultats du séquençage génomique en aval en dressant un portrait plus complet de la tumeur grâce aux échantillons obtenus. Nous pensons que, grâce à elle, nous aurons une meilleure chance de déceler toutes les mutations derrière le cancer, ce qui aidera les cliniciens à choisir le meilleur traitement », dit M. Fenster. Cette technologie mise au point au Robarts Research Institute de London a un autre avantage, soit celui de pouvoir être utilisée avec les types de systèmes ultrasoniques que l’on retrouve couramment dans les hôpitaux, ce qui permet de réduire les coûts et de supprimer les autres obstacles à son adoption en pratique clinique.
Le codirecteur du programme d’imagerie de l’IORC, et homologue de M. Fenster, est M. Martin Yaffe, docteur en biophysique médicale, qui travaille au Sunnybrook Research Institute de Toronto où il est en train de mettre au point des traceurs moléculaires novateurs pour l’imagerie de différents types de cancer. Ces traceurs sont conçus pour permettre la détection de sous-ensembles de cellules cancéreuses et, lorsqu’ils sont utilisés avec l’information obtenue par des techniques d’imagerie comme l’IRM, peuvent servir à guider le choix des traitements qui ciblent ces cellules et à surveiller leur efficacité.
« Étudier l’hétérogénéité spatiale des tumeurs par imagerie est un concept relativement novateur. Autrefois, nous n’avions pas les mêmes outils pour déceler les différences à l’intérieur d’une tumeur de façon aussi détaillée qu’aujourd’hui. Notre groupe ainsi que nos collaborateurs de l’initiative d’oncologie adaptative s’efforcent de comprendre comment ces différences spatiales, observées au fil du temps, expliquent pourquoi certains cancers réapparaissent après avoir été traités et pourquoi d’autres ne répondent jamais complètement au traitement dès le départ », explique M. Yaffe.
Les nouvelles frontières de la pathologie : l’étude du cancer cellule par cellule
Les améliorations en imagerie et en technologie génomique saluées par MM. Fenster, Stein et Yaffe ont contribué dans une large mesure à rendre possible la révolution actuelle dans le domaine des soins et de la recherche en cancérologie. Cependant, l’un des progrès les plus stupéfiants a sans doute été réalisé dans un domaine qui existe depuis des centaines d’années, soit celui de la pathologie.
M. John Bartlett, docteur en physiologie de la reproduction et directeur du programme de développement diagnostique de l’IORC, explique comment la pathologie du cancer évolue et de quelle façon cette transformation touche l’oncologie adaptative.
« Actuellement, les pathologistes étudient les cellules au microscope pour voir à quel point elles ont dévié de leur apparence normale. Grâce à son expérience et à la reconnaissance des formes, le pathologiste détermine dans quelle mesure le tissu est désorganisé et attribue au cancer un grade fondé sur ce degré de désorganisation. L’un des problèmes que posent ces méthodes classiques est qu’un cancer de bas grade ressemble beaucoup à des cellules normales », dit M. Bartlett. Selon lui, bien que la pathologie classique demeurera essentielle à l’établissement d’un diagnostic dans les prochaines décennies, les nouvelles techniques que ce groupe et d’autres comme lui sont en train de mettre au point s’y ajouteront et permettront de poser un diagnostic beaucoup plus exact et précis.

« Ce que nous faisons, c’est ajouter à la pathologie classique une nouvelle dimension. Grâce à l’analyse d’images, il est maintenant possible d’examiner et de produire des données sur la longueur, la largeur, l’intensité de la coloration, la forme et d’autres caractéristiques de chaque cellule d’un cancer. Il s’agit de la même démarche, mais nous utilisons maintenant des ordinateurs pour mieux voir. »
À l’aide de données sur des millions de cellules cancéreuses provenant de milliers de patients, M. Bartlett et son équipe recherchent des caractéristiques de taille et de forme susceptibles de les aider à interpréter de façon plus précise un échantillon fourni par un pathologiste traditionnel. De plus, le groupe est en mesure de colorer les cellules d’un échantillon pour rechercher plusieurs protéines spécifiques. Par exemple, un échantillon de cancer du sein pourrait être coloré pour mettre en évidence les cellules qui expriment le récepteur des œstrogènes, le récepteur de la progestérone, l’oncogène HER2 et un marqueur de prolifération appelé KI67.
Ce que nous faisons, c’est ajouter à la pathologie classique une nouvelle dimension. Grâce à l’analyse d’images, il est maintenant possible d’examiner et de produire des données sur la longueur, la largeur, l’intensité de la coloration, la forme et d’autres caractéristiques de chaque cellule d’un cancer.
– M. John Bartlett
« Actualiser les technologies en pathologie nous a permis d’interroger les cancers d’une toute nouvelle façon, en nous attardant à la taille et à la forme des cellules ainsi qu’à l’expression intégrée des protéines cellule par cellule comme nous ne l’avions jamais fait auparavant, explique M. Bartlett. En pratique clinique, être capable de comprendre ces cancers cellule par cellule et de voir les différences à l’intérieur de la tumeur permettrait d’obtenir des renseignements précieux pour le choix du traitement et la prévention des récidives par la surveillance des patients. »
Trouver les signes cardinaux d’un cancer aux premiers stades de son développement
Être en mesure de comprendre l’évolution des tumeurs permet non seulement d’obtenir des renseignements précieux pour orienter le traitement, mais aussi de déceler les tumeurs de manière précoce lorsqu’elles sont petites et traitables. Au moyen de technologies de séquençage novatrices qui leur permettent de remonter le temps jusqu’aux origines des tumeurs et à leurs premières mutations, les chercheurs du programme d’oncologie adaptative recherchent les signes cardinaux génétiques d’un cancer aux premiers stades de son développement.
« L’une des façons que nous avons de déterminer les caractéristiques associées à un cancer aux premiers stades de son développement est d’étudier les milliers d’échantillons de sang fournis par les participants de l’Étude sur la santé Ontario, dit le Dr Stein. Nous séquençons ces échantillons puis nous recoupons ces résultats avec les dossiers médicaux et d’autres données pour voir s’il y a des changements évolutifs précoces communs chez les personnes atteintes de cancer. »
La découverte de ces caractéristiques moléculaires peut permettre de concevoir de nouvelles façons de dépister les personnes susceptibles d’avoir un cancer plus tard au cours de leur vie. Celles-ci peuvent être ensuite aiguillées vers les programmes de dépistage indiqués de manière à ce qu’un éventuel cancer puisse être traité dès les premiers stades de son développement.
Mieux comprendre le cancer pour améliorer la prévention, le diagnostic et les soins
À mesure que les chercheurs dévoilent la complexité des cellules cancéreuses, il devient de plus en plus nécessaire de répondre aux questions posées par la recherche en faisant appel aux compétences de spécialistes des diverses disciplines de l’oncologie. L’initiative d’oncologie adaptative mobilise les riches ensembles de données provenant de cohortes canadiennes, les technologies de biopsie liquide de l’IORC et les compétences de l’Ontario en imagerie de précision pour réaliser, dans le domaine de la recherche sur le cancer, des percées que l’on pourra rapidement adapter et qui permettront de conserver une longueur d’avance sur la maladie.
« Mener des recherches à l’époque d’un tel changement transformationnel de la technologie et être au premier rang quand vient le temps de procurer les bienfaits de ces outils aux patients de l’Ontario et du monde entier est passionnant, affirme le Dr Stein. Nous sommes fiers d’avoir réuni certains des meilleurs chercheurs en cancérologie de la province pour mettre en pratique le concept d’oncologie adaptative. Grâce à notre approche multidisciplinaire, nous nous efforçons de produire de réelles innovations qui aideront de nombreux patients à vivre plus longtemps et en meilleure santé que ce que laissait entrevoir le diagnostic initial. »